2022年8月30日、若手研究者と企業等の交流・連携機会の創出を目的としたマッチングイベント「第5回メドテックマッチング 若手研究者による最新技術を用いた人工臓器・ウイルス検査機器開発」がオンラインで行われました。このイベントでは、本事業に採択された2名の先生がスピーカーとなり、ご自身の研究に関する講演を行いました。
冒頭ではモデレーターの前田より事業説明をいたしました。
家庭で毎日ウイルス等を検査可能なスクリーニングキット技術基盤の開発
鵜澤 尊規
1台で治療・診断・予防を行う人工知能を備えた人工心臓の研究開発
土方 亘

ゲストスピーカー

理化学研究所
専任研究員
鵜澤 尊規
研究分野:拡張型進化分子工学を使った機能性ペプチドの創出
講演の内容
2022年8月の第5回メドテックマッチングでは、スピーカーとして理化学研究所 専任研究員でいらっしゃいます鵜澤尊規先生をお招きして、オンラインにて講演を開催いたしました。今回の講演では「家庭で毎日ウイルス等を検査可能なスクリーニングキット技術基盤の開発」というテーマでお話いただきました。
冒頭のお話は「新型コロナウイルス感染症の検査方法の現状と課題」についてです。
現在、新型コロナウイルスの検査では、主に「PCR検査」と「抗原検査」が使用されています。PCR検査は、精度は高いですが検査結果が出るまでに1時間ほどかかり、抗原検査は、PCR検査に比べて精度は劣るものの15分ほどで済むといった特徴があります。
課題として、検査数が増えると検査機関がキャパオーバーしてしまう点や、感染症とそれに伴う世界の混乱は今後も定期的に発生する可能性があり、その度に対応を考えなければならないという点が挙げられます。
こういった課題を解決するため、最近では個人で検査をすることが推奨され、抗原検査キットの増産計画も進められています。しかし、増産まで時間がかかることや、増産時の部材の供給、増産後の在庫管理に関する問題点も残っています。
鵜澤先生は、残された問題点を解決できる次世代の感染症検出キットとして「高感度・高信頼性」はもちろんの事、「シンプルに、少ない部材で量産できる高い即応性」「低価格・個人利用が可能」といった要件が重要であると考えています。
次に、鵜澤先生が研究されている「Binding enhanced fluorogenicペプチド(BEFペプチド)」と、それを利用した感染症検出キットの開発についてお話いただきました。
BEFペプチドとは、新型コロナウイルスやインフルエンザウイルスなど、特定のターゲットに結合した場合のみ蛍光を発するペプチドです。環境応答性の蛍光色素を使用しており、例えばNBDという蛍光色素の場合は、周りを水に囲まれていると蛍光が出ないもの、水と離れる事で蛍光を発するという原理を利用します。
また、特定のターゲットに結合するペプチドは、リボソームディスプレイと呼ばれる方法で選出します。膨大な量のDNAライブラリを用意し、配列を転写・翻訳するのですが、その際に蛍光発生型非天然アミノ酸を入れることで、蛍光物質を持ったペプチドを作り出すことができます。その状態で、特定のターゲットに結合するペプチド配列情報を持つRNAを回収してDNAに戻す作業を繰り返し、BEFペプチドを選出します。
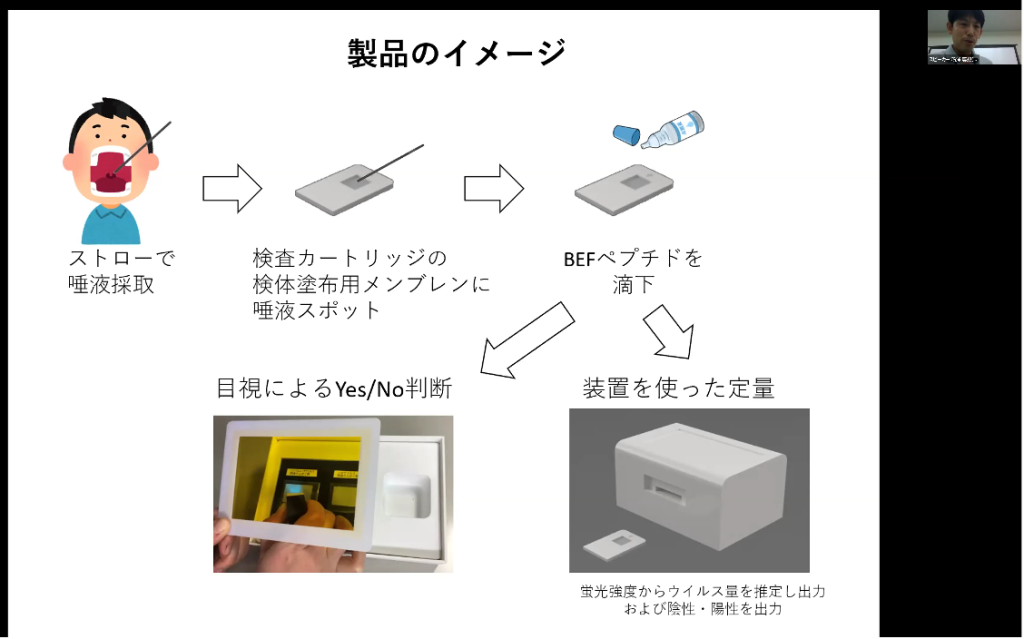
このBEFペプチドを使った感染症検出キットのイメージについても説明いただきました。ストローで採取した唾液を検査カートリッジに落とし、その上にBEFペプチドを滴下します。その後、目視または装置を使って検査を行うというものです。
BEFペプチド検査の分子認識の要となるアプタマーは化学合成で簡単に作ることができ、検出装置も安価かつ少ない部材点数で生産することができます。
これは、鵜澤先生が考える「高い即応性」「低価格・個人利用が可能」という課題解決の要件を満たしています。
また、リードアウトはPCR検査と同様の蛍光を使うことから、「高感度・高信頼性」も維持することが可能です。
今後はPOCを行うことで感度を確かめ、医療機器メーカーやハード設計会社の方との共同研究で実用化を目指しています。
最後に設けられた質問コーナーでは「BEFペプチド検査の所要時間はどのくらいか」「抗原検査で検出できない無症状患者や発症直後の患者にも適応可能なのか」「現行品と比較して感度や価格の差はどのくらいになるのか」などたくさんの質問が寄せられ、丁寧にお答えいただきました。
鵜澤先生、ご講演ありがとうございました。

ゲストスピーカー

東京工業大学
准教授
土方 亘
研究分野:体内発電システム、体内非接触給電、人工皮膚等の研究開発
講演の内容
2022年8月の第5回メドテックマッチングでは、スピーカーとして東京工業大学 准教授でいらっしゃいます土方亘先生をお招きして、オンラインにて講演を開催いたしました。今回の講演では「1台で治療・診断・予防を実現する人工知能を備えた人工心臓」というテーマでお話いただきました。
最初に、人工心臓をとりまく状況についてお話いただきました。
心臓の病気で亡くなる方の割合は世界における死亡原因の中で最も多く、例えば、アメリカでは心不全を患っている方は約570万人、そのうち約90万人の方が毎年亡くなっています。心不全の治療法としては心臓移植が最も有効ですが、1年のあいだに心臓移植を受けることができるのは2,300人程度と、かなり少ないのが現状です。このように、心不全を患っているにもかかわらず心臓移植を受けることができない方々を救うため、人工心臓は使われています。
人工心臓にはさまざまなタイプがありますが、近年では、インペラを非接触で支持する磁気浮上型のものがメインになってきています。磁気浮上型は、回転部に摩耗が生じないため耐久性が高く、血液に優しい点が特徴です。
アメリカにおいて人工心臓は、心臓移植が適用できるかどうかを判断するまで、または心臓移植手術を実施するまでの橋渡しとして使用されることもありますが、圧倒的に多いのは、心臓移植をせず半永久的に人工心臓で生きる最終的治療法Destination Therapy(DT)としての使用です。日本ではDTとしての使用はまだ少ないですが、昨年より保険適用が始まったこともあり、今後増えていくことが予測されます。
また、移植までの橋渡しの場合、病院でサポートを受けながら人工心臓を使うことが一般的でしたが、DTとなると在宅での治療が前提となります。人工心臓自体が治療・診断・予防を行い、医師の助けとなるような「人工知能を備えた人工心臓」が必要になってくると土方先生は考えています。
次は、人工心臓の課題についてお話いただきました。
DTとして人工心臓を植え込んだ後の生存率を見てみると、1年後には2割、5年後には5割の方が亡くなっており、決して生存率が高いとは言えません。
人工心臓植え込み後の有害事象として、血栓・出血が多いことが挙げられます。人工心臓は人工物なので、血液に接すると血栓ができやすいという特徴があります。なるべく血栓ができないよう構造や材料を工夫しているものの、完全に防ぐことは難しく、抗凝固療法を行うこともあります。抗凝固材は血液を固まりにくくするものですが、使用量によっては出血を引き起こしてしまうのです。
合併症や心不全の悪化による再入院が多いことも有害事象の一つです。人工心臓は一定の回転数で疾患心臓の流量を補助しますが、一定の流量が出続けることにより大動脈弁が正常に開かず、血栓ができるという合併症が生じることがあります。
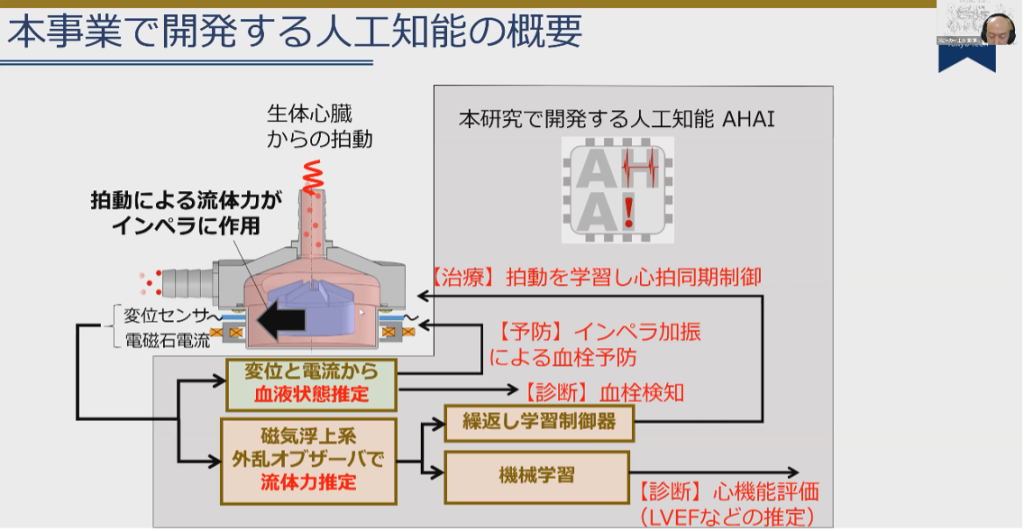
後半では、課題を解決するため、土方先生が研究開発を進めている「人工知能を備えた人工心臓」の概要についてお話いただきました。
血栓を解決する方法として、磁気浮上型人工心臓のインペラを揺らすことで、すでに搭載されている変位センサ・電磁石電流から血液状態を推定し、早い段階で血栓を検知する機能を研究しています。さらに、インペラが加振する動作そのもので血栓を予防する機能についても研究を進めており、どちらも有効な実験結果が確認できています。
また、合併症予防や心機能を回復させるため、「心拍同期制御」というシステムの実現も目指しています。人工心臓が生体心臓の拍動のタイミングを学習し、拍動に合わせてモーターの回転数を上げたり、落としたりする仕組みです。これによって心臓の流量に変化が出るので、大動脈弁が正常に開くようになり、合併症の予防に繋がります。この心拍同期制御については、生体内へセンサを追加することなく、人工心臓にすでに備わっているシステムと人工知能のインストールのみで実現できるよう研究を進めています。
最後に設けられた質問コーナーでは「血栓を検知した際、排除する機能は組み込まれるのか」「心拍同期制御を行うシステムは患者ごとに必要なのか、もしくは1台で数名の患者を管理できるのか」「他の病気の治療への応用法はあるか」など、たくさんの質問が寄せられ、丁寧にお答えいただきました。
土方先生、ご講演ありがとうございました。
